Customer Updates: Stryker Network Disruption > Read Now
Deutscher Kongress für Orthopädie und Unfallchirurgie
Ein umfassendes Portfolio für Orthopäden und Neurochirurgen, die auf Wirbelsäulenchirurgie spezialisiert sind.
Unser ständig wachsendes Portfolio bietet Lösungen für die Wirbelsäule, die vom Okziput bis zum Becken reichen.
MIS-Pedikelschrauben-System.
Effizient. Einfach. Sicher.
Wir haben dieses System gemeinsam mit Chirurgen entwickelt, um Effizienz, Einfachheit und Sicherheit für MIS-Verfahren zu bieten. ES2 bietet Ihnen eine low-Profile Fixationslösung zusammen mit rationalisierter Instrumentierung, die es Ihrem Team erleichtert, sich um Ihre Patienten zu kümmern.
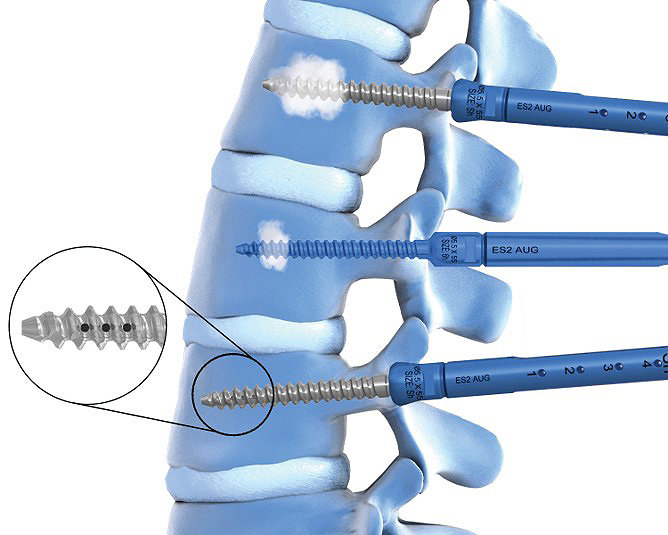
- Integrierte Bladekonstruktion mit 15 mm eingebauten Reduktionsgewinden
- Der Ring ermöglicht eine präzise Stabkonturierung dank seiner sicheren Fixierung an der Schraube und seiner Fähigkeit, an verschiedenen Punkten entlang des Blades angebracht zu werden
- Geeignet für sowohl ∅5.5 als auch ∅6.0 mm vorgeschnittene gerade und vorgebogene Titanstäbe für die Behandlung mehrerer Pathologien mit einem System
- Die Schrauben weisen drei Schneidekerben auf, um das Einbringen zu erleichtern, sowie ein kortikales Spongiosa-Gewindemuster, das auf die Anatomie des Pedikels abgestimmt ist und einen starken Halt im Pedikel ermöglicht
- Innovative Instrumentierung für einfache Handhabung
- Kompatibel mit Bohr- und Navigationsfunktionen

unvergleichbare Mobilität
Ein hochmobiler CT-Scanner mit der größten verfügbaren Gantry Öffnung zur Gewährleistung der chirurgischen Gesamtgenauigkeit und eines hocheffizienten Arbeitsablaufs
Ein hochmobiler diagnostischer 32-Schicht-CT-Scanner, der die hohen Anforderungen in der Notfallradiologie unterstützt, indem er potenziell zeitsparende diagnostische Bildgebung in hoher Qualität bietet
- Kann eine schnellere klinische Entscheidungshilfe bei zeitkritischen Behandlungen bieten
- Bietet einen noch nie dagewesenen Zugang zum Patienten mit der größten verfügbaren Öffnung (107 cm)
- 51,2 cm Sichtfeld und 1 m Scanbereich bieten vollständige Visualisierung des Torsos mit einer einzigen spiralförmigen Abtastung
- Benutzerdefinierte Protokolle bieten eine Anpassung und Feinabstimmung für schraubenförmige wie auch axiale CT-Scan-Erfassungstechniken
- intraoperatives CT als die technisch fortschrittlichste Variante der intraoperativen Schichtbilddarstellung *
- intraoperative Darstellung mit nahezu diagnostischer Qualität **
- Verringerung der Revisionsrate bei Beckenoperationen um 4,4% **
- niedrigere Artefakt-Raten **
- Standardprotokolle für Becken und Extremitäten verfügbar
- Verwendung nicht auf den OP beschränkt
- postoperativer Kontrollscan direkt im OP möglich
Trotz ähnlicher chemischer Eigenschaften verhalten sich viele Produkte aufgrund ihrer verschiedenen Strukturen unterschiedlich. Vitoss hat eine offene, miteinander verbundene Struktur, die die 3-D-Knochenregeneration begünstigt. 1
Nur Materialien mit interkonnektierender Porosität ermöglichen eine 3-D-Regeneration des Knochens. Darüber hinaus hat sich gezeigt, dass eine erhöhte Porosität zu einer höheren Fusionsrate des Knochens führt (in einem Tiermodell). Vitoss ist ein hochporöses Kalziumphosphat (bis zu 90% porös).2
- Der Zusatz von bioaktivem Glas trägt zur Schaffung einer für die Osteoblasten Befestigung günstigen Oberfläche bei8
- Die Vitoss BA-Knetmasse ist in einer flüssigen Umgebung stabil, kann das Knochenmark aufsaugen und halten, und ist formbar
- Der Vitoss BA Streifen ist im feuchten Zustand flexibel, kann das Knochenmark aufsaugen und halten, ist kompressionsbeständig und leicht zu schneiden
Die Literatur zum Wirkungsmechanismus Bioaktiven Glases zeigt, dass es sich im Tiermodell gut mit dem Knochen verbindet.3 Bei der Implantation werden die ionischen Bestandteile (Silizium, Natrium und Kalzium) des bioaktiven Glases in die Umgebung freigesetzt und reagieren mit Körperflüssigkeiten.4 Diese Reaktion bewirkt die Ablagerung einer dünnen Schicht von physiologischem Kalziumphosphat an seiner Oberfläche, was die Anheftung der Osteoblasten begünstigt.5 Dies wird allgemein als bioaktiver Effekt bezeichnet.6 Dies kann zur Bindung von neuem Knochen an das Material führen. Vitoss BA verfügt über eine einzigartige Porosität, Struktur und Chemie, um die 3D-Regeneration von Knochen voranzutreiben. Die Zugabe von bioaktivem Glas trägt dazu bei, eine für die Osteoblasten Anlagerung günstige Oberfläche zu schaffen und unterstützt das Implantat bei der Regeneration von neuem Knochen.7

Die Tritanium-In-Growth-Technologie wurde für den Knochenfusion und die biologische Fixierung entwickelt.9
Die einzigartige poröse Struktur ist darauf ausgelegt, ein günstiges Umfeld für die Anheftung und Proliferation von Zellen zu schaffen.10,11 Tritanium-Material kann im Vergleich zu herkömmlichem Titan in der Lage sein, Flüssigkeit aufzunehmen oder zurückzuhalten.12 Inspiriert von der Mikrostruktur der Spongiosa11 und ermöglicht durch AMagine, Strykers urheberrechtlich geschützte Vorgehensweise bei der Herstellung von Implantaten mittels additiver Fertigung, ist diese Technologie bewusst auf Fusion ausgelegt.


Die MESA 2-Schrauben der nächsten Generation sind von oben belastbar, haben ein low Profile und sind mit der Zero-Torque Technology ausgestattet. Das rationalisierte Instrumentarium ist auf Effizienz und schnellere Einbringung ausgelegt. Dieses System ist darauf ausgerichtet, die schwierigsten Korrekturmanöver bei komplexen Wirbelsäulenpathologien zu bewältigen.
Das Mesa 2 Cricket macht die Notwendigkeit von Repositionsschrauben praktisch überflüssig, da es eine Reduktion von 27 mm bietet und eine simultane multiaxiale Translation und Reposition ermöglicht. Mesa 2 gewährt dem Chirurgen die Flexibilität und Sicherheit, die er benötigt, um Deformationsoperationen mit einer DDC-Technik durchzuführen.
- Dual-lead Gewinde für schnelleres Einbringen der Schraube
- Zero-Torque Technology
- Kein Profil oberhalb der Stange
- Einstufige endgültige Verriegelung über den Mesa-2-Crickets
- Das revolutionäre Design des Crickets ermöglicht Korrekturmanöver in allen Ebenen sowie eine schnelle Entfernung
- Einzigartige Instrumentierung zur langsamen, kontrollierten Korrektur der Wirbelsäule bei gleichzeitiger Verteilung der Kräfte auf das gesamte Konstrukt
- Fähigkeit zur segmentalen oder umfassenden Derotation der Wirbelsäule, um eine Korrektur in der axialen Ebene zu erreichen
In situ extrahierbares Korpektomie-Cage System
Das thorako-lumbal expandierbare Korpektomie-Cage-System Capri bietet eine innovative Lösung zur Stabilisierung der Wirbelsäule bei Wirbelkörperresektionen infolge eines Traumas oder Tumors. Dieses vielseitige System wird in verschiedenen Profiloptionen angeboten und ermöglicht eine in-situ-Höhenanpassung und Endplattenabwinkelung.
Capri Cervical 3D Expandable wird mit der lamellaren 3D-Titantechnologie konstruiert. Diese Technologie umfasst 500 μm Porenkanäle im gesamten Implantat, die in Verbindung mit Querfenstern ein miteinander verbundenes Gitter bilden, das die knöcherne Integration ermöglicht.13
- Mehrere chirurgische Zugänge möglich
- In-situ-Lordose und Kyphose-Angulation
- In-situ höhenverstellbar
- Austauschbare Profiloptionen
- Hergestellt aus Titan


Pedikelschrauben mit Dual Lead Gewinde, True-Tip-Technologie und einer einzigartigen Verzahnung (Serration).
Diese einzigartige Schraubenfamilie zeichnet sich durch die True-Tip-Technologie, ein Dual-Lead-Gewinde und 24 umlaufende Serrationen an der distalen Spitze der Schraube aus. Ihr kortikales spongiöses Gewindemuster ist eine Fortsetzung unserer klinisch bewährten Xia-Designphilosophie und wurde entwickelt, um die Leistung und den Halt sowohl in kortikalem als auch in spongiösem Wirbelknochen zu maximieren.
Kontakt
References
Die Umgebung, in der Airo eingesetzt werden soll, erfordert eineangemessene Abschirmung zum Schutz von Strahlung. EineAnleitung zur Strahlungsabschirmung finden Sie in der MobiusAiro Vorinstallationsanleitung. Eine Beurteilung durch lokalanerkannte Experten für Strahlungskontrolle kann ebenfallserforderlich sein. Der medizinischen Fachkraft obliegt dieEntscheidung für oder gegen die Verwendung bestimmterProdukte und Operationstechniken im individuellen Patientenfall.Stryker erteilt insofern keinen medizinischen Rat und empfiehlteingehende Produktschulungen und Trainings vor der Verwendungder jeweiligen Produkte.
1. Orthovita Test Report P/N 1050-0003R.
2. Orthovita Test Report P/N 1070-0008R.
3. Hench, L.L., Splinter, R.J., and Allen, W.C., Bonding Mechanisms at the Interface of Ceramic Prosthetic Materials. Journal of Biomedical Materials Research, 1971; 2(1): 117-141; Hench, L.L., Paschall, H.A., Direct Chemical Bond of Bioactive Glass-Ceramic Materials to Bone and Muscle. Journal of Biomedical Materials Research, 1973; 4: 25-42; Gross, U., The Interface of Various Glasses and Glass Ceramics with a Bony Implantation Bed. Journal of Biomedical Materials Research, 1985; 19: 251-271
4. Hench, L.L., The Story of Bioglass. Journal of Materials Science: Materials in Medicine, 2006 Nov; 17(11): 967-78; Oonishi, H., et al., Particulate Bioglass Compared with Hydroxyapatite as a Bone Graft Substitute. Clinical Orthopaedics and Related Research, 1997 Jan; 334: 316-25; Vrouwenvelder, W.C.A., Histological and Biochemical Evaluation of Osteoblasts Cultured on Bioactive Glass, Hydroxyapatite, Titanium Alloy, and Stainless Steel. Journal of Biomedical Materials Research, 1993 Apr; 27(4): 465-75; Xynos, I.D., Edgar, A.J., Buttery, L.D.K., Hench, L.L., and Polak, J.M., Ionic Products of Bioactive Glass Dissolution Increase Proliferation of Human Osteoblasts and Induce Insulin-like Growth Factor II mRNA Expression and Protein.
5. Hench, L.L., Polak, J.M., Xynos, I.D., Buttery, L.D.K., Bioactive Materials to Control Cell Cycle. Materials Research Innovations, 2000; 3(6): 313-323
6. Hench, L.L., Splinter, R.J., and Allen, W.C., Bonding Mechanisms at the Interface of Ceramic Prosthetic Materials. Journal of Biomedical Materials Research, 1971; 2(1): 117-141; Hench, L.L., Paschall, H.A., Direct Chemical Bond of Bioactive Glass-Ceramic Materials to Bone and Muscle. Journal of Biomedical Materials Research, 1973; 4: 25-42; Gross, U., The Interface of Various Glasses and Glass Ceramics with a Bony Implantation Bed. Journal of Biomedical Materials Research, 1985; 19: 251-271; Vrouwenvelder, W.C.A., Histological and Biochemical Evaluation of Osteoblasts Cultured on Bioactive Glass, Hydroxyapatite, Titanium Alloy, and Stainless Steel. Journal of Biomedical Materials Research, 1993 Apr; 27(4): 465-75; . Sanders, D.M., Hench, L.L., Mechanisms of Glass Corrosion. Journal of American Ceramic Society.1973; 56(7): 373-377; Hench, L.L., Characterization of Glass Corrosion and Durability. Journal of Non-Crystalline Solids, 1975; 19: 27-39; Ogino, M., Hench, L.L., Formation of Calcium Phosphate Films on Silicate Glasses. Journal of Non-Crystalline Solids, 1980; 38 and 39: 673-678.
7. Hench, L.L., Splinter, R.J., and Allen, W.C., Bonding Mechanisms at the Interface of Ceramic Prosthetic Materials. Journal of Biomedical Materials Research, 1971; 2(1): 117-141; Hench, L.L., Paschall, H.A., Direct Chemical Bond of Bioactive Glass-Ceramic Materials to Bone and Muscle. Journal of Biomedical Materials Research, 1973; 4: 25-42; Gross, U., The Interface of Various Glasses and Glass Ceramics with a Bony Implantation Bed. Journal of Biomedical Materials Research, 1985; 19: 251-271; Vrouwenvelder, W.C.A., Histological and Biochemical Evaluation of Osteoblasts Cultured on Bioactive Glass, Hydroxyapatite, Titanium Alloy, and Stainless Steel. Journal of Biomedical Materials Research, 1993 Apr; 27(4): 465-75; . Sanders, D.M., Hench, L.L., Mechanisms of Glass Corrosion. Journal of American Ceramic Society.1973; 56(7): 373-377; Hench, L.L., Characterization of Glass Corrosion and Durability. Journal of Non-Crystalline Solids, 1975; 19: 27-39; Ogino, M., Hench, L.L., Formation of Calcium Phosphate Films on Silicate Glasses. Journal of Non-Crystalline Solids, 1980; 38 and 39: 673-678.
8. Hench, L.L., Splinter, R.J., and Allen, W.C., Bonding Mechanisms at the Interface of Ceramic Prosthetic Materials. Journal of Biomedical Materials Research, 1971; 2(1): 117-141.
Hench, L.L., Paschall, H.A., Direct Chemical Bond of Bioactive Glass-Ceramic Materials to Bone and Muscle. Journal of Biomedical Materials Research, 1973; 4: 25-42.
Gross, U., The Interface of Various Glasses and Glass Ceramics with a Bony Implantation Bed. Journal of Biomedical Materials Research, 1985; 19: 251-271.
Vrouwenvelder, W.C.A., Histological and Biochemical Evaluation of Osteoblasts Cultured on Bioactive Glass, Hydroxylapatite, Titanium Alloy, and Stainless Steel. Journal of Biomedical Materials Research, 1993 Apr; 27(4): 465-75
Sanders, D.M., Hench, L.L., Mechanisms of Glass Corrosion. Journal of American Ceramic Society.1973; 56(7): 373-377.
Hench, L.L., Characterization of Glass Corrosion and Durability. Journal of Non-Crystalline Solids, 1975; 19: 27-39.
Ogino, M., Hench, L.L., Formation of Calcium Phosphate Films on Silicate Glasses. Journal of Non-Crystalline Solids, 1980; 38 and 39: 673-678.
9. PROJ43909 | Tritanium technology claim support memo. Data on file.
10. RD0000053710 | Tritanium cell infiltration and attachment experiment. Data on file.
11. Karageorgiou V, Kaplan D. Porosity of 3D biomaterial scaffolds and osteogenesis. Biomaterials 2005;26: 5474–91.
12. RD0000050927 | Tritanium material capillary evaluation. Data on file
13. K2M Test Report TR-1220
Content ID: MIES2-WB-1_14882, GEN-SS-9_Rev-1_24567, TruCT-SS-1_24582, TruCT-BR-6_24576, PRTBI-BR-1 ddm/SC/GS, BIVIT-WB-3_Rev-1_16203, TRITA-WB-2_Rev-1_15842, PRTDF-WB-3_20637, K2-62-7008-01, PRTTT-WB-1_Rev-1_24327, PRTCV-WB-16_20712, TLSER-WB-1_14898
